Esta técnica de Reprodução Assistida muitas vezes é confundida com a Fertilização in Vitro (FIV). Porém, é um procedimento muito mais simples do que a FIV. A inseminação artificial com sêmen do marido (homóloga) está indicada para casais cuja causa de esterilidade esteja relacionada a fatores que impeçam os espermatozoides de chegarem até a cavidade uterina.
Dentre estes, encontramos casos de impotência, orifício uretral peniano fora do lugar (epi ou hipospadia), ejaculação em direção à bexiga (ejaculação retrógrada), sêmen com contagem baixa de espermatozoides (oligospermia), espermatozoides com baixa motilidade (atenospermia), homens que congelaram sêmen antes de realizar vasectomia, radioterapia ou quimioterapia, vaginismo, fator cervical, ou ainda esterilidade sem causa aparente (ESCA).
A intenção do procedimento é otimizar as condições de encontro dos espermatozoides com o óvulo, já que os melhores espermatozoides são selecionados através de técnica de laboratório chamada Capacitação, e colocados dentro do útero, injetados através de uma pequena cânula, sendo este um procedimento indolor.
Além disso, a capacitação melhora a movimentação dos espermatozoides, os quais serão inseminados no momento mais próximo à ovulação. Esta ovulação também será melhorada/potencializada por medicamentos específicos para indução da ovulação.
PROCEDIMENTO E TÉCNICA
Antes de iniciar um tratamento de inseminação artificial, há necessidade de realizar um exame chamado CAPACITAÇÂO. Este exame verificará se a quantidade e qualidade do sêmen é adequada para a realização de uma inseminação. A seguir, considerando que a mulher não tenha nenhum problema, será induzida a ovulação da esposa com medicamentos à base de citrato de clomifeno (Serofene, Indux ou Clomid) e gonadotrofinas (Gonal, Fostimon, Menopur, Puregon etc).
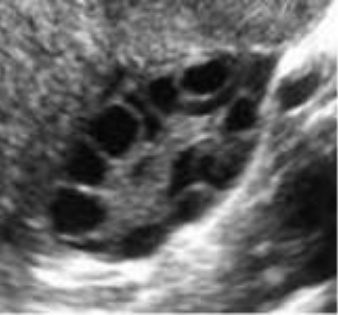
A indução é controlada através de ultrassonografias que mostrarão quando os folículos estariam próximos da ovulação. Neste dia, utiliza-se uma dose de hCG (Ovidrel, Choragon, Choriomon) para induzir a ruptura folicular e realizar a inseminação nas próximas horas.
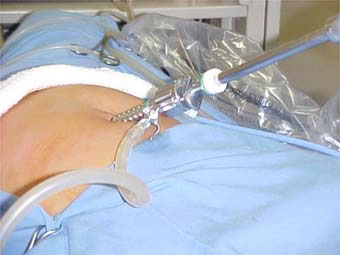
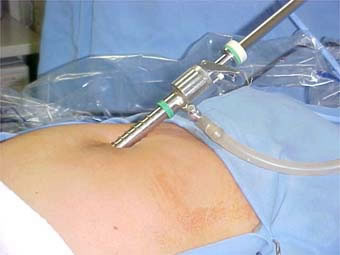
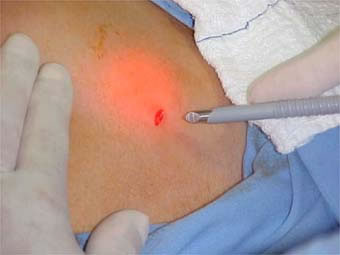
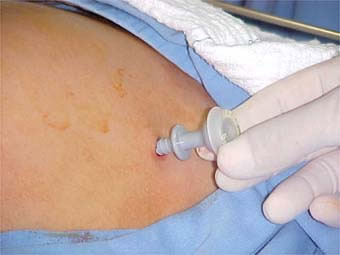
No dia marcado para a inseminação, o marido faz a coleta no laboratório, ou em casa, e traz para o laboratório, para logo ser processada realizando sua Capacitação. Este procedimento demora cerca de duas horas.
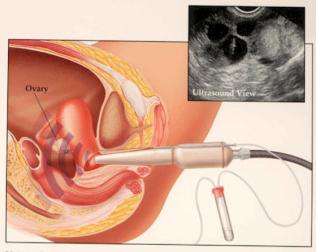
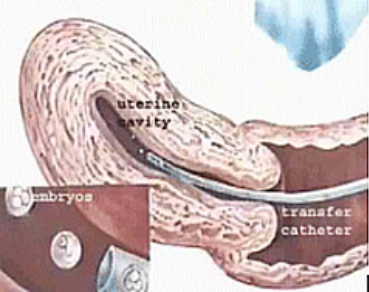
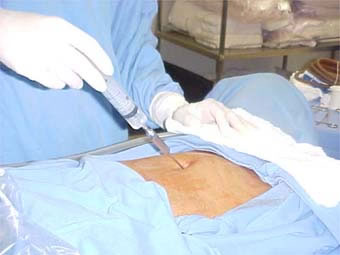
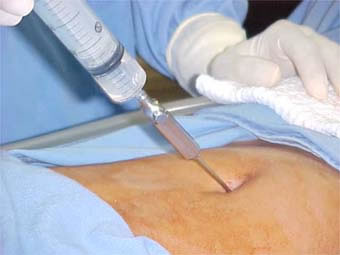
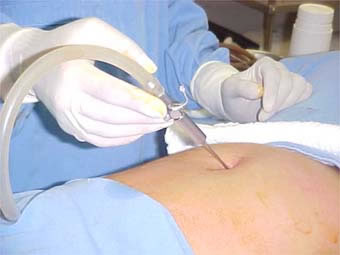
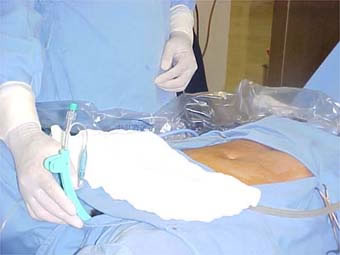
Quando pronto o sêmen capacitado, a esposa será posicionada de maneira similar a um exame ginecológico. Será inserido um espéculo vaginal até visualizar o colo uterino. Uma antissepsia, com algodão e soro fisiológico, será realizada para evitar carregar microorganismos para dentro da cavidade uterina. Uma seringa acoplada a um cateter de plástico (similar à agulha comprida) é carregada com o sêmen preparado do marido. A ponta deste cateter é introduzida pelo canal do colo uterino até atingir a cavidade. Neste momento, o preparado de sêmen é injetado. Após alguns segundos, a cânula é retirada, retira-se o espéculo e deixamos a paciente deitada por alguns minutos.
O tempo entre o início da indução e a realização da inseminação é de aproximadamente 12 a 14 dias. Duas semanas mais tarde, saberemos se o tratamento deu certo.
O teste de gravidez chama-se Beta-hCG. As chances de sucesso desta técnica dependem do motivo da indicação e da idade da mulher. Pode variar de 5%, nos casos de qualidade espermática ruim, até 16% em casos de fator cervical ou esterilidade sem causa aparente.
PRÉ-REQUISITOS DO CASAL
Para a mulher: As trompas deverão estar permeáveis e funcionais. Estas características podem ser avaliadas por Histerossalpingografia ou por Videolaparoscopia. Porém, a funcionalidade só poderá ser confirmada se a paciente engravidar, não havendo testes para investigação desta característica.
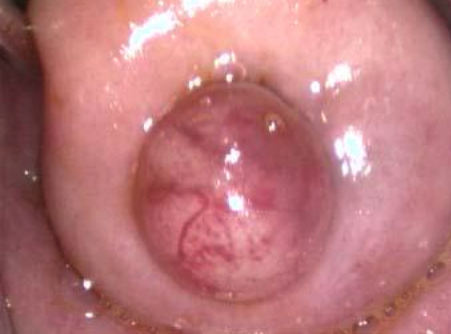
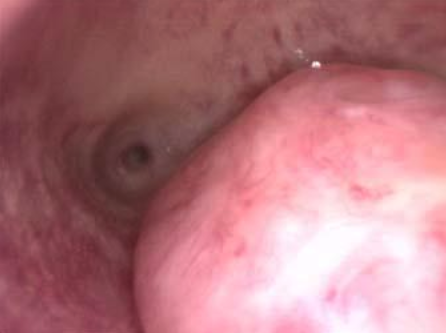
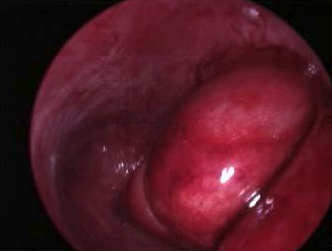
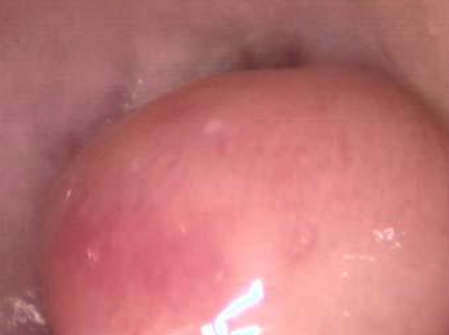
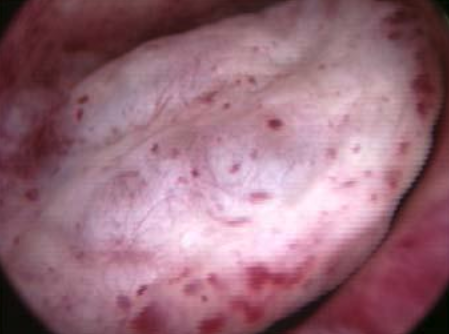
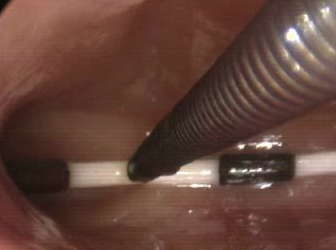
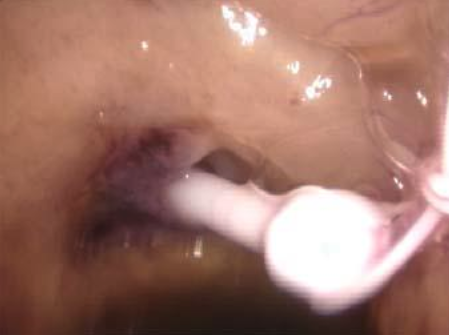
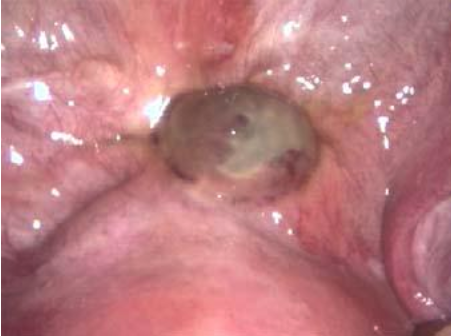
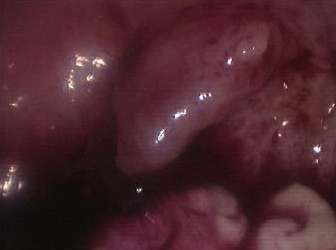
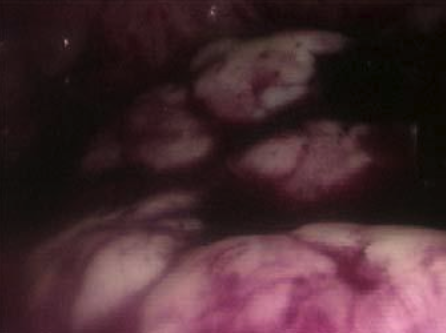
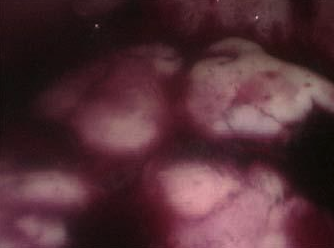
A cavidade uterina deverá ser livre de lesões como: pólipos, miomas, sinéquias, septo e endometrite. (Imagens destas lesões podem ser vistas em Videohisteroscopia). Quando houver endometriose, deverá ser tratada antes de realizar a inseminação. Também é necessária a existência de, pelo menos, um ovário que produza folículos e que, se possível, responda à estimulação medicamentosa (indução de ovulação).